Concetti Chiave
- Gli atomi sono le particelle più piccole di un elemento con proprietà chimiche distintive e sono composti da protoni, neutroni ed elettroni.
- Il modello di Rutherford paragona l'atomo a un sistema solare, con il nucleo al centro composto da protoni e neutroni, mentre gli elettroni orbitano attorno ad esso.
- Il numero di protoni nel nucleo di un atomo determina la sua massa atomica e le sue proprietà chimiche e fisiche.
- Gli isotopi sono varianti di atomi con lo stesso numero di protoni ma un diverso numero di neutroni.
- Gli ioni sono atomi che hanno perso o guadagnato elettroni, acquisendo una carica positiva o negativa.
In questo contenuto si parlerà della realtà che ci circonda formata da particelle invisibili. Vedremo come l'intuizione di Dalton abbia aperto la strada a una comprensione profonda della materia, passando per il fascino del modello "planetario" di Rutherford fino a capire perché alcuni atomi pesano più di altri o possiedono una carica elettrica.
L'atomo secondo Dalton: l'unità fondamentale
Il viaggio verso il cuore della materia inizia con John Dalton, un chimico inglese che per primo ebbe l'intuizione corretta. Ogni elemento della natura è composto da minuscole unità identiche tra loro, che chiamò “atomi”. Se volessimo dare una definizione semplice, l'atomo è la parte più piccola di un elemento che ne mantiene intatte le caratteristiche chimiche. Immaginiamolo come il "mattone" fondamentale: se lo dividessimo ulteriormente, non avremmo più quell'elemento specifico ma solo pezzi di materia generica.Quando questi mattoni si incastrano tra loro attraverso reazioni chimiche, creano le molecole. Una molecola si forma dall'unione di due o più atomi che decidono di viaggiare insieme per formare sostanze più complesse. Alcuni esempi sono l'ossigeno che respiriamo o l'acqua.
Formazione interna di un atomi
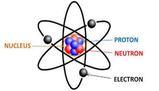
La scienza ha scoperto che all'interno dell' atomo c'è un'organizzazione complessa fatta di tre particelle subatomiche principali:- Il Protone: si trova nel centro dell'atomo e ha una carica elettrica positiva.
- Il Neutrone: abita anch'esso nel centro, ma come dice il nome è "neutro", ovvero non ha carica elettrica.
- L'Elettrone: è una particella leggerissima, molto più piccola delle altre due, dotata di carica negativa.
Identità chimica e il concetto di orbitale
Ogni tipo di atomo ha un numero fisso di protoni nel suo nucleo. Questo numero è fondamentale perché decide quanto l'atomo sia capace di attirare elettroni e quale sia la sua massa totale. In pratica, è il numero di protoni a stabilire se un atomo si comporterà come un metallo, come un gas o come un solido.C'è però un dettaglio importante sul movimento degli elettroni: non seguono binari precisi come i treni. Poiché si muovono a velocità incredibili, essi creano quello che i chimici chiamano orbitale. L'orbitale non è una linea, ma una zona di spazio intorno al nucleo dove è molto probabile trovare l'elettrone in un dato momento. Questi spazi si distribuiscono a diverse distanze dal centro, formando vari livelli energetici.
Le varianti della materia: Isotopi e Ioni
Non tutti gli atomi dello stesso elemento sono uguali. Anche se il numero di protoni non cambia mai, il numero di neutroni può variare. Questi "gemelli" dello stesso elemento, che pesano in modo diverso ma si comportano chimicamente allo stesso modo, si chiamano isotopi. Molti di essi sono fondamentali in medicina e nella ricerca storica (come il famoso Carbonio-14).Infine, l'atomo può subire variazioni che riguardano gli elettroni. Quando un atomo ne perde o ne acquista uno o più, perde la sua neutralità. Se ha più elettroni del normale avrà una carica negativa. Invece se ne ha meno, avrà una carica positiva. Questa differenza di carica è il motore di moltissime reazioni e permette loro di legarsi per formare nuovi composti.






 Accedi a tutti gli appunti
Accedi a tutti gli appunti
 Tutor AI: studia meglio e in meno tempo
Tutor AI: studia meglio e in meno tempo