Concetti Chiave
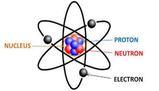
- L'atomo è composto da particelle subatomiche: protoni, neutroni ed elettroni.
- I protoni hanno carica positiva, i neutroni sono neutri e gli elettroni hanno carica negativa.
- Il numero di massa atomica (A) è la somma di protoni e neutroni nell'atomo.
- Il numero atomico (Z) corrisponde al numero di protoni ed elettroni, ed è uguale per entrambi.
- Gli elettroni occupano orbitali attorno al nucleo, partendo dal livello energetico più basso.
L'atomo
L’atomo è una particella a sua volta composta da particelle più piccole, chiamate subatomiche e sono: protoni, neutroni ed elettroni.
Il protone ha carica unitaria positiva, mentre il neutrone nulla, tuttavia le loro masse sono confrontabili, ossia il numero di elettroni e di protoni, all’interno di un atomo, coincide. Gli elettroni hanno invece una massa molto piccola e carica unitaria negativa.
Considerato un atomo abbiamo due numeri ad esso associabili:
• Di massa atomica: dato dalla somma dei protoni e dei neutroni. Esso si indica con la lettera A.
• Atomico: dato dal numero di protoni ed elettroni, che deve essere uguale. Quindi se un atomo ha sei protoni e sei elettroni, allora il numero atomico sarà 6 e lo si indicherà con la lettera Z.
Protoni ed elettroni compongono il nucleo, mentre gli elettroni si trovano negli orbitali, regioni di spazio che appunto orbitano attorno al nucleo. Ogni orbitale costituisce un certo livello energetico, su cui possono trovarsi al massimo due elettroni. L’orbitale più vicino al nucleo si trova ad livello energetico basso, ed è il primo ad essere occupato dagli elettroni; quello più lontano avrà un alto livello energetico e sarà l’ultimo ad essere occupato. Dunque, gli elettroni di un atomo occupano gli orbitali dal livello più basso a quello più alto.


 Accedi a tutti gli appunti
Accedi a tutti gli appunti
 Tutor AI: studia meglio e in meno tempo
Tutor AI: studia meglio e in meno tempo