Concetti Chiave
- L'atomo è la più piccola parte di un elemento che ne conserva le caratteristiche ed è composto da particelle subatomiche: elettroni, neutroni e protoni.
- Il nucleo dell'atomo contiene protoni (cariche positive) e neutroni (neutre), mentre gli elettroni (cariche negative) ruotano attorno al nucleo in orbitali.
- Gli orbitali, che determinano la probabilità di trovare un elettrone, sono classificati in quattro tipi: s, p, d, f, e formano sette livelli energetici.
- Gli elettroni di valenza, con maggiore energia, occupano il guscio di valenza e determinano le proprietà chimiche dell'atomo.
- Il numero atomico (Z) indica il numero di protoni ed elettroni, mentre il numero di massa (A) è la somma di protoni e neutroni; gli isotopi variano nel numero di massa.
L'atomo è l'unità fondamentale della materia ,essendo la più piccola parte dell'elemento ,che ne conserva le caratteristiche. Esso risulta composto da particelle dette subatomiche : elettroni , neutroni , protoni.
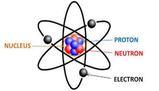
Essenzialmente è spazio vuoto , ma nel Nucleo troviamo i protoni ( particelle cariche positivamente) e neutroni ( particelle neutre) . Attorno al nucleo ruotano invece gli elettroni ( particelle cariche negativamente) , secondo una traiettoria , non definita , detta orbitale (zona dove è massima la probabilità di trovare un elettrone) .
Gli orbitali sono 4 e sono chiamati s,p,d,f .
Gli elettroni risultano disposti intorno al nucleo a seconda dell'energia che possiedono ( maggiore è l'energia posseduta , maggiore è la distanza dal nucleo) . Creando cosi 7 livelli energetici .
* per allontanare un elettrone dal nucleo e portarlo ad uno strato più esterno, occorre fornire all'atomo una quantità di energia pari alla differenza di energia che c'è tra i due livelli . Se l'energia non basta , dato che non ci sono livelli intermedi , l'elettrone tornerà al livello di partenza , liberando l'energia precedentemente assorbita . Gli elettroni con maggiore energia , detti elettroni di valenza , occupano il guscio di valenza .
In un atomo il numero dei protoni è uguale a quello degli elettroni : l'atomo si dice per questo , elettricamente neutro.
- Numero atomico (Z) : somma dei protoni presenti nell'atomo ( e di conseguenza di elettroni).
- Numero di massa ( A) : Somma dei protoni più neutroni (nucleoni).
per conoscere il numero dei neutroni : A-Z.
La massa di una particella subatomica è espressa in unità di massa atomica dette Dalton.
*Isotopi : atomi dello stesso elemento che si differenziano per il numero di massa . Il nome isotopo deriva dal fatto che essi si trovano nello stesso posto nella tavola periodica .
Domande da interrogazione
- Quali sono le particelle subatomiche che compongono un atomo?
- Come si determina il numero di neutroni in un atomo?
- Cosa sono gli isotopi e come si differenziano tra loro?
Un atomo è composto da elettroni, neutroni e protoni. I protoni e i neutroni si trovano nel nucleo, mentre gli elettroni orbitano attorno al nucleo.
Il numero di neutroni si determina sottraendo il numero atomico (Z) dal numero di massa (A), ovvero A-Z.
Gli isotopi sono atomi dello stesso elemento che si differenziano per il numero di massa, pur avendo lo stesso numero di protoni.



 Accedi a tutti gli appunti
Accedi a tutti gli appunti
 Tutor AI: studia meglio e in meno tempo
Tutor AI: studia meglio e in meno tempo