Concetti Chiave
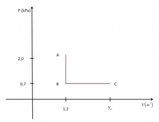
- Il gas perfetto subisce una trasformazione ciclica con due isoterme (BC e DA) e due isobare (AB e CD).
- Le temperature delle trasformazioni isoterme sono calcolate utilizzando l'equazione di stato dei gas perfetti e la costante di Boltzmann.
- La temperatura nel tratto BC è calcolata come 72,6 K, mentre nel tratto DA è di 11,1 K.
- I volumi negli stati A e C sono determinati usando la legge di Boyle, con valori di 6,83 x 10^-3 m^3 e 6,32 x 10^-4 m^3 rispettivamente.
- Le trasformazioni cicliche coinvolgono variazioni di pressione e volume, mentre la temperatura rimane costante nelle isoterme.

I valori del volume e della pressione negli stati B e D sono:
- Calcola il valore delle temperature [math]T_1[/math]e[math]T_2[/math]a cui avvengono le due trasformazioni isoterme.
- Calcola il valore del volume negli stati A e C della trasformazione.
Quesito 1
Per prima cosa, trasformiamo i valori del volume nella giusta unità di misura:
Per calcolare la temperatura nei tratti in cui avviene la trasformazione isoterma consideriamo l'equazione di stato dei gas perfetti:
dove n è il numero di moli.
Poiché noi abbiamo il numero di molecole possiamo sfruttare la formula
dove
Sostituiamo questa formula all'equazione di stato dei gas perfetti:
Notiamo che la formula può essere scritta anche in questo modo:
Abbiamo quindi un quoziente fra due costanti:
Sostituiamo la pressione e il volume nel punto B per calcolare la temperatura a cui avviene la trasformazione nel tratto BC:
Quindi abbiamo:
Allo stesso modo calcoliamo la temperature nel tratto DA:
Quesito 2
Per calcolare il volume negli stati A e C consideriamo che le trasformazioni nei tratti BC e AD sono isoterme, cioè a temperatura costante. Possiamo quindi utilizzare la legge di Boyle:
Quindi:
Poiché nel tratto CD la pressione è costante, la pressione nello stato c è uguale a quella nello stato D.
Allo stesso modo calcoliamo il volume nello stato A, tenendo presente che la pressione in quello stato è uguale a quella nel punto B:
Domande da interrogazione
- Come si calcolano le temperature delle trasformazioni isoterme nel ciclo del gas perfetto?
- Qual è la temperatura nel tratto BC della trasformazione isoterma?
- Come si determina il volume negli stati A e C della trasformazione?
- Qual è il volume nello stato C?
Le temperature delle trasformazioni isoterme si calcolano utilizzando l'equazione di stato dei gas perfetti, [math]pV = Nk_BT[/math], sostituendo i valori di pressione e volume nei punti specifici del ciclo.
La temperatura nel tratto BC è calcolata come [math]T_{BC} = \frac{p_B V_B}{N k_B}[/math], risultando in 72,6 K.
Il volume negli stati A e C si determina utilizzando la legge di Boyle, [math]p_0 V_0 = pV[/math], considerando che le trasformazioni BC e AD sono isoterme.
Il volume nello stato C è calcolato come [math]V_C = \frac{p_B V_B}{p_C}[/math], risultando in [math]6,83 \cdot 10^{-3} m^3[/math].


 Accedi a tutti gli appunti
Accedi a tutti gli appunti
 Tutor AI: studia meglio e in meno tempo
Tutor AI: studia meglio e in meno tempo