Concetti Chiave
- Il concetto di Orbitale rappresenta la probabilità del 90% di trovare un Elettrone in una regione di spazio.
- Tre Numeri Quantici descrivono le caratteristiche degli Orbitali: Principale (n), Angolare (l) e Magnetico (m).
- Gli Orbitali si dividono in quattro tipi: s (sferici), p (simili a due gocce d'acqua), d, e f, con forme e valori di l differenti.
- Il Principio di Esclusione di Pauli afferma che un Orbitale può contenere al massimo due Elettroni con spin opposto.
- L'energia di un Orbitale è influenzata sia dal Numero Quantico Principale (n) che dal Numero Quantico Angolare (l).
-Gli Orbitali-
Per spiegare i comportamenti e i movimenti degli Elettroni, venne introdotto dagli scienziati il concetto di Orbitale, il quale è quella regione di spazio in cui vi è la probabilità pari al 90% di poter trovare un Elettrone.
Le Caratteristiche degli Orbitali sono dettate da tre Numeri Quantici:
• Il Numero Quantico Principale (simbolo n), descrive le Dimensioni e l’Energia dell’Orbitale; può assumere tutti i valori interi positivi compresi tra 1 ed infinito.
• Il Numero Quantico Angolare (simbolo l), indica la Forma dell’Orbitale; può assumere tutti i valori interi compresi tra 0 e (n – 1).
• Il Numero Quantico Magnetico (simbolo m), indica le diverse possibilità di Orientazione degli Orbitali dello spazio; può assumere tutti i valori compresi tra –l e +l.
• Esiste anche un altro Numero Quantico, quello di Spin, che si riferisce al Senso di Rotazione dell’Elettrone; può assumere solo i valori -½ e ½.
Esistono quattro tipi di Orbitali: gli Orbitali s, p, d, f.
Gli Orbitali s hanno valore di l = 0; sono simili ad una nube elettronica di forma sferica.
Gli Orbitali p hanno valore di l = 1; hanno forma simile a quella di due gocce d’acqua.
Gli Orbitali d hanno valore di l = 2.
Gli Orbitali f hanno valore di l = 3.
Il fisico austriaco Wolfgang Pauli enunciò il Principio di Esclusione, secondo il quale in un unico Orbitale non vi possono essere più di due Elettroni e, se ve ne sono due, essi devono avere numero quantico di spin opposto.
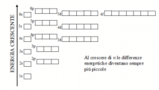
L’Energia degli Orbitali dipende sia dal Numero Quantico Principale (n) che dal Numero Quantico Angolare (l).






 Accedi a tutti gli appunti
Accedi a tutti gli appunti
 Tutor AI: studia meglio e in meno tempo
Tutor AI: studia meglio e in meno tempo